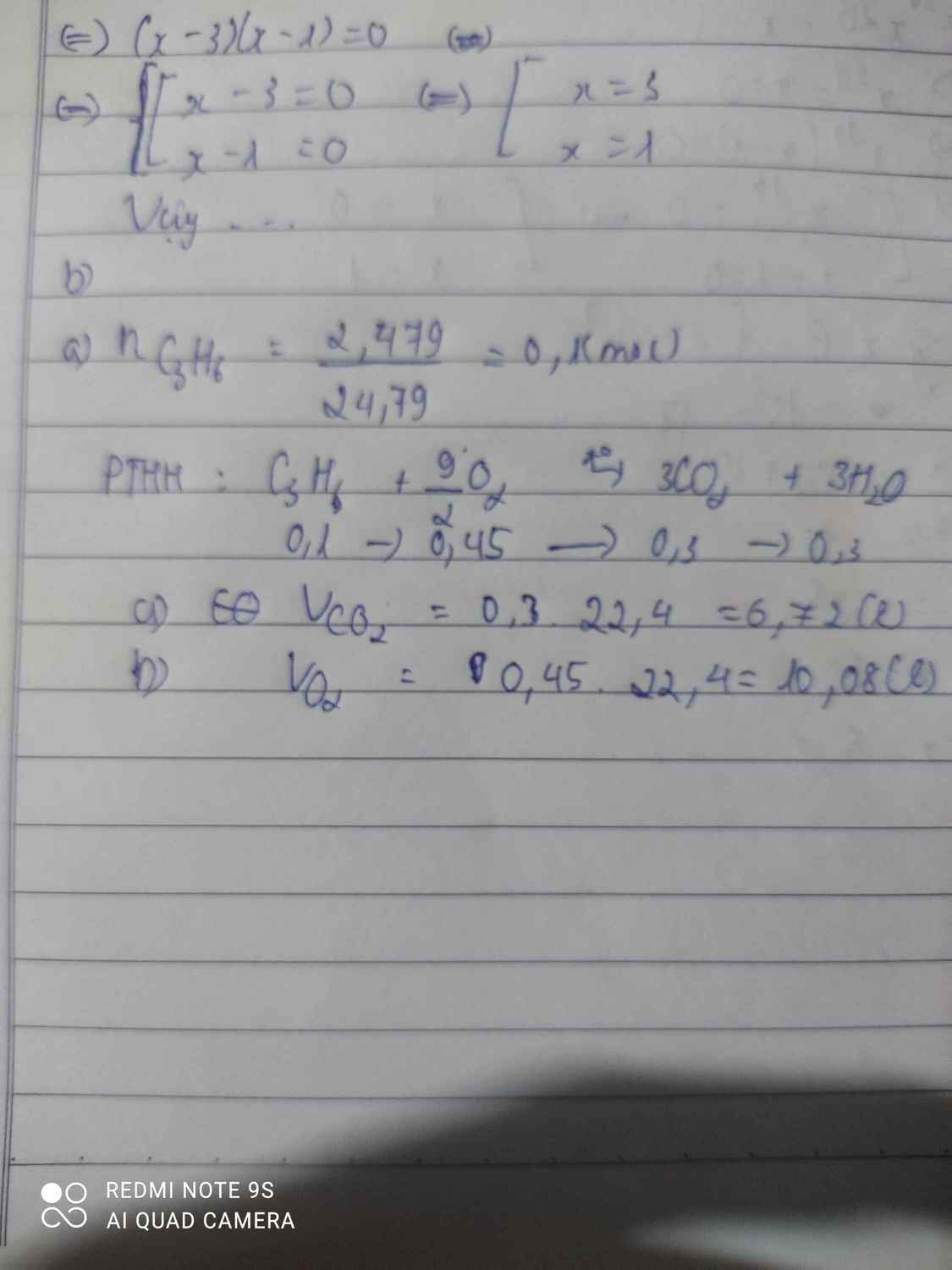đốt cháy hoàn toàn 11,2 lit khí methane hãy tính khí oxygen cần dùng và thể tích khí carbonic tạo thành ( ở đkc 25°C , 1bar ) xin có giải thích , vì sao luôn ạ

Những câu hỏi liên quan
. Đốt cháy hoàn toàn 6,1975 lít hỗn hợp khí gồm methane và acethylene (đkc) cần dùng 14,874 lít khí oxygen (đkc).
a) Tính % V mỗi khí trong hỗn hợp đầu.
b) Tính tổng thể tích khí CO2 sinh ra (đkc). Cho C =12, H =1
CH4+2O2-to>CO2+2H2O
x-----------2x
C2H4+3O2-to>2CO2+2H2O
y------------3y
=>\(\left\{{}\begin{matrix}x+y=0,25\\2x+3y=0,6\end{matrix}\right.\)
=>x=0,15 mol
y=0,1 mol
=>%CH4=\(\dfrac{0,15.24,79}{6,1975}\).100=60%
=>%C2H4=40%
=>VCO2=(0,15+0,2).24,79=8,6765l
Đúng 1
Bình luận (0)
đốt cháy 2,479 lít propane trong khí oxygen (đkc) thì thu được khí carbonic và hơi nước
a. Tính thể tích khí CO2 thu được.
b. Tính thể tích khí oxygen cần dùng.
n C3H8=0,1 mol
C3H8+5O2-to>3CO2+4H2O
0,1-----0,5------------0,3-----0,4 mol
=>VCO2=0,3.22,4=6,72 l
=>VO2=0,5.22,4=11,2l
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 11,2 lit khí etilen ( C2H4 ) tạo ra sản phẩm CO2 và H2O
a) tính thể tích khí oxi cần dùng ở phản ứng trên
b) tính thể tích không khí cần dùng, biết khí oxi chiếm ⅕ thể tích không khí. Biết thể tích khi ở điều kiện tiêu chuẩn
a, \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Ta có: \(n_{C_2H_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Theo PT: \(n_{O_2}=3n_{C_2H_4}=1,5\left(mol\right)\Rightarrow V_{O_2}=1,5.22,4=33,6\left(l\right)\)
b, \(V_{kk}=\dfrac{V_{O_2}}{20\%}=168\left(l\right)\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 11,2 lit khí etilen ( C2H4 ) tạo ra sản phẩm CO2 và H2O
a) tính thể tích khí oxi cần dùng ở phản ứng trên
b) tính thể tích không khí cần dùng, biết khí oxi chiếm s thể tích không khí. Biết thể tích khi ở điều kiện tiêu chuẩn
PTHH: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(n_{C_2H_4}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
Theo PTHH: \(n_{O_2}=3.n_{C_2H_4}=3.0,5=1,5\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=1,5.22,4=33,6\left(l\right)\)
câu b oxi chiếm bao nhiêu của kk vậy bạn
Đúng 2
Bình luận (2)
Đốt cháy hoàn toàn 11,2 lít khí metan. Hãy tính thể tích khí oxi cần dùng và thể tích khí cacbonic tạo thành. Biết các thể tích khí đo ở điều kiện tiêu chuẩn.
a) Những khí tác dụng với nhaư từng đôi một là:
CH4 và O2; CH4 và Cl2; H2 và O2; H2 và Cl2.
b) Những hỗn hợp nổ là những hỗn hợp khi phản ứng tỏa nhiều nhiệt, đó là các hỗn hợp: CH4 và O2; H2 và O2
Đúng 0
Bình luận (1)
Phương trình phản ứng
CH4 + 2O2 -> CO2 + 2H2O
nCH4 =11,2/22,4=0,5 mol
theo phương trình phản ứng : nCH4=2nO2 =>nO2=0,5.2=1 mol
VO2=n.22,4=1.22,4=22,4 l
nCO2=0,5 mol
=>VCO2=n.22,4=0,5.22,4=11,2 l
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn "37.185" (lit) khi Acetylene ( C2H2) ở ( đkc) trong không khí. a. Viết phương trình hóa học của phản ứng. b. Tính thể tích không khi cần dùng để đốt cháy hết lượng khi acetylene trên. Các thể tích được do ở (đkc). Biết oxygen chiếm 20% thể tích không khi. c. Nếu cho toàn bộ sản thu được qua bình dựng dung dịch nước vôi trong Ca(OH), dư, thì thu được bao nhiêu gam kết tủa.
Đốt cháy hoàn toàn 2,479 lit khí CO thu đc khí CO2. Tính thể tích khí O2 cần dùng các khí đó ở đkc
\(2CO+O_2\rightarrow\left(t^o\right)2CO_2\\ n_{CO}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\\ n_{O_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ V_{O_2\left(đkc\right)}=0,05.24,79=1,2395\left(l\right)\)
Đúng 0
Bình luận (0)
mình cùng ko bt thế này đúng ko
2CO+O2→(to)2CO2nCO=2,47924,79=0,1(mol)nO2=0,12=0,05(mol)VO2(đkc)=0,05.24,79=1,2395(l)
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 3,36 lít khí etilen(ở đkc)
A)tính thể tích khí oxi cần dùng ở đkc
B)tính thể tích khí cacbonic được tạo thành ở đkc
C)đẫn khí cacbonic tạo thành qua bình đựng nước vôi trong dư, thi thu được một kết tủa A. Tính khối lượng của kết tủa A
Cho C=12 ;H=1 ;O=16 ;Ca=40
Xem chi tiết
a, PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Ta có: \(n_{C_2H_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{O_2}=3n_{C_2H_4}=0,45\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,45.22,4=10,08\left(l\right)\)
b, Theo PT: \(n_{CO_2}=2n_{C_2H_4}=0,3\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,3.22,4=6,72\left(l\right)\)
c, PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{\downarrow}=m_{CaCO_3}=0,3.100=30\left(g\right)\)
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Đốt 32 gam khí CH4 trong không khí thu được khí CO2 và hơi nước.
a. Tính khối lượng khí CO2 thu được
b. Tính thể tích khí oxygen cần dùng (ở 25oC, 1bar)
(chú ý: ở ĐKC(25oC,1bar) thì Vkhí = n. 24,79)
a,\(n_{CH_4}=\dfrac{32}{16}=2\left(mol\right)\)
PTHH: CH4 + 2O2 --to→ CO2 + 2H2O
Mol: 2 1 2
\(\Rightarrow m_{CO_2}=2.44=88\left(g\right)\)
b,\(V_{O_2}=1.24,79=24,79\left(l\right)\)
Đúng 0
Bình luận (0)